عوامل ایجادکنندهی ( infectious arthritis آرتریت عفونی یا septic septic و عفونی هر دو به یک معنا هستند 🙂
۱٫ باکتریها (شایعترین)
۲٫ گنوکوک
۳٫ ویروسها
۴٫ قارچها
۵٫ توبِرکُلوز.
۶٫ الیم (نوعی اسپیروکت)
نکاتی چند:
Neisseria gonorrhoeae ، s.oureus و سایر باکتریها شایعترین عوامل ایجادکنندهی آرتریت عفونی هستند.
عفونتهای حاد باکتریایی به طور معمول یک مفصل یا تعداد کمی از مفاصل را درگیر میکنند.
مونوآرتریت و الیگوآرتریت تحت حاد یا مزمن غالباً توسط عفونتهای mycobacterial یا قارچی ایجاد میشود.
در بیماریهای سیفیلیس، الیم و reactive arthritis التهاب ایجاد شده به صورت episodic میباشد.
عوامل ایجادکنندهی ( acute polyarticular inflammation التهاب حاد چند مفصلی ) ۵ مفصل یا بیشتر :
۱٫ اندوکاردیت
۲٫ تب روماتیسمی
۳٫ disseminated neisserial infection )عفونت نایسریایی منتشر(
۴٫ acute hepatitis B
۵٫ باکتریها و ویروسها ( البته اینها acute polyarticular inflammationرا بیشتر در افراد مستعد ) مانند افرادِ مبتال به آرتریت روماتوئید ایجاد میکنند.
عوامل ایجادکنندهی ( acute monoarticular arthritis ) آرتریت حاد تک مفصلی :
۱٫ S.aureus
۲٫ S.pneumonie
۳٫ β-hemolytic streptococci
۴٫ باسیلهای گرم منفی
۵٫ نایسریا گونوره
۶٫ گونههای کاندیدا
۷٫ crystal-induced arthropathy )نقرس، شبه نقرس(
۸٫ خونریزی مفصلی )hemarthrosis(
۹٫ اجسام خارجی
۱۱٫ osteoarthritis )آرتروز(
۱۲٫ نکروز ایسکمی
۱۳٫ آرتریت روماتوئید تک مفصلی
عوامل ایجادکنندهی ( chronic monoarticular arthritis ) آرتریت مزمن تک مفصلی :
۱٫ ( mycobacterium tuberculosis )شایعترین
۲٫ non-tuberculosis mycobacterium مانند بورلیا، کاندیدا، بروسال و …
۳٫ osteoarthritis
۴٫ :Legg–Calvé–Perthes disease : شروع این بیماری در دوران کودکی است به این صورت که جریان خون در عروق خونرسان به سر استخوان femur مختل میشود و باعث avascular necrosis یا همان osteonecrosis میگردد که در نهایت استخوان میمیرد و رشد آن متوقف میشود.
عوامل ایجادکنندهی ( polyarticular arthritis ) آرتریت چند مفصلی ۵ مفصل یا بیشتر :
۱٫ مِنَنگوکوک.
۲٫ گنوکوک
۳٫ غیر گنوکوکی
۴٫ اندوکاردیت باکتریال
۵٫ قارچها
۶٫ هپاتیت B
۷٫ parvovirus ها
۸٫ HIV
۹٫ rubella virus
۱۱٫ sickle cell disease
۱۲٫ reactive arthritis
۱۳٫ ( Poncet’s disease نوعی reactive arthritisِ ناشی از توبرکلوز میباشد.
۱۴٫ serum sickness
۱۵٫ تب روماتیسمی حاد
۱۶٫ بیماریهای التهابی روده
۱۷٫ لوپوس
۱۸٫ آرتریت روماتوئید
۱۹٫ واسکولیت
۲۰٫ سارکوئیدوز
نکته: برای ارزیابی مفصلی که دچار التهاب است بایدحتماً آسپیراسیون مایع مفصلی انجام دهیم که در اکثر موارد خیلی کار سختی نخواهد بود. آسپیراسیون را با یک سوزن ضخیم ( large-bore needle ) از نواحیای که بیشترین fluctuation یا tenderness و راحتترین دسترسی را دارد انجام میدهیم.
گاهی اوقات انجام آسپیراسیون کمی سخت میشودمثالً؛ زمانهایی که مفصل عمقیتر و دسترسی به آن کمتر باشد )مفاصلی همچون shoulder، hip، …(، در این مواقع میتوانیم از ultrasonography و fluoroscopy کمک بگیریم.
تعداد سلولهای مایع مفصلی به طور نرمال باید زیر ۱۸۱ سلول به ازای هر میکرولیتر باشد. غالب این سلولها از نوع mononuclear cell میباشند. در یکسری موارد تعداد سلولهای مایع مفصلی افزایش مییابد:
۱) در acute bacterial infection، تعداد سلولهای مایع مفصلی به ۲۵۱۱۱-۲۵۱۱۱۱ سلول به ازای هر میکرولیتر میرسد )میانگین: .)۱۱۱۱۱۱ cells/µl در این بین بیش از %۹۱ سلولها نوتروفیل خواهد بود.
۲) در موارد نقرس )crystal-induced arthropathy(، آرتریت روماتوئید و آرتریتهای التهابی غیر عفونی این تعداد بین ۳۱۱۱۱-۵۱۱۱۱ سلول به ازای هر میکرولیتر خواهد بود.
۳) در عفونتهای mycobacterial و قارچی این تعداد به ۱۱۱۱۱-۳۱۱۱۱ سلول به ازای هر میکرولیتر میرسد که در این بین %۵۱-۷۱ آنها نوتروفیل و بقیهشان لنفوسیت است.
برای تشخیص قطعی آرتریت عفونی یا همان septic کارهای زیر را انجام میدهیم:
۱٫ شناسایی عامل پاتوژن موجود در مایع مفصلی گرفته شده.
۲٫ ایزوالسیون عامل پاتوژن شناخته شده از کشت مایع مفصلی.
۳٫ انجام PCR و بررسی نوکلئیک اسیدهای عامل پاتوژن که به تشخیص خیلی کمک میکند.
پاتوژنز آرتریت باکتریایی حاد:
عامل باکتریایی ایجادکنندهی آرتریت از راههای مختلفی به مفصل میرسد. خون، بافت نرم یا استخوان عفونی اطراف مفصل، تلقیح مستقیم هنگام انجام جراحی و همچنین تروما همگی راههایمختلف ِمنتقل شدنِ باکتری و عفونت به مفصل میتوانند باشند.
معموالً در ابتدا نوتروفیلها و باکتریها وارد فضای مفصلی میشوند و بعد باکتریها به غضروف مفصلی متصل میشوند. به دنبال این ورود و اتصال و تهاجم، فشار داخل مفصلی افزایش مییابد و پروتئازها و سیتوکینهایی از کندروسیتها و ماکروفاژهای مفصلی آزاد میشود. همهی این موارد گفته شده دست به دست هم میدهند تا در عرض ۴۸ ساعت، تخریب غضروفی آغاز شود.
مطالعات بافتشناسی نشان دادهاند که این عوامل باکتریایی با پوشاندن synovium و غضروف مفصلی )cartilage( آبسههایی ایجاد میکنند که به داخل synovium، غضروف مفصلی و در موارد شدیدتر به داخل استخوانِ subchondral کشیده میشوند.
در ادامهی ماجرا synovial proliferation رخ میدهد که در نتیجهی آن، ترومبوز عروق مفصلی و ساختاری به نام pannus تشکیل میشود. pannus چیست؟ طبق اینترنت ، یک الیه از بافت fibrovascular یا granulation است که به صورت غیر طبیعی به روی مفصل تشکیل میگردد )مثالً در آرتریت روماتوئید، reactive arthritis و …(.
میکروبیولوژی آرتریت باکتریایی حاد:
شایعترین راه منتقل شدن عفونت به مفصل در تمام سنین راه خونی ( hematogenous ) است.
در نوزادان ( infants ) ، استرپتوکوکهای گروه B، باسیلهای گرم منفی و S.aureus پاتوژنهای معمول هستند.
از زمان ساخته شدن واکسنِ هموفیلوس آنفوالنزا، S.aureus و S.pyogenes )استرپتوکوک گروه )A در بین کودکان زیر ۵ سال شایع شده است.
در افراد بزرگسال و بالغین شایعترین عامل ایجادکنندهی آرتریت septic، N.gonorrhoeae یا همان گنوکوک است.
در بالغین در مواردی که عامل ایجادکنندهی آرتریت gonococcal نباشد یعنی non-gonococcal باشد، S.aureus شایعترین عامل خواهد بود.
باسیلهای گرم منفی، پنوموکوک و استرپتوکوک (β-hemolyticخصوصاً گروههای A و )B عامل ۱/۳ از آرتریتهای septic در افراد مسنتر است به خصوص آنهایی که یک بیماری زمینهای )comorbid disease( هم دارند.
عامل آرتریتهای عفونی ایجاد شده به دنبال جراحی یا آسیبهای نفوذی )penetrating injuries( در بیشتر موارد S.aureus است و در برخی موارد هم سایر باکتریهای گرم مثبت و باسیلهای گرم منفی میباشد.
در افرادی که پروتز مفصل داشتهاند و یا arthroscopy شدهاند، استافیلوکوک کوآگوالز منفی عامل ایجادکنندهی آرتریت septic آنها است. در بقیهی افراد این باکتری عاملی نادر است.
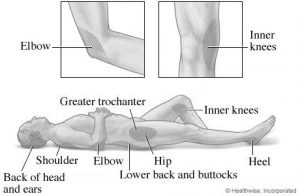
ارگانیسمهای بیهوازی را زمانی در مفاصل میبینیم که فرد گاز گرفته شود و یا decubitus ulcer و آبسه intraabdominal یک فرد به مفصل مجاورش انتشار پیدا کند. decubitus ulcer چیست؟ طبق اینترنت فشار طوالنی مدت به روی پوست باعث ایجاد آن میشود. عکس روبهرو نواحیای که احتمال decubitus ulcer در آنها بیشتر است را به ما نشان میدهد.
گازی که گربه و یا سایر حیوانات میگیرند و یا scratch ای که ایجاد میکنند میتواند باعث ورود عامل pasteurella multocida به مفصل گردد.
اپیدمیولوژی آرتریت باکتریایی حاد:
درحالی که S.aureus، H.influenzae و S.pyogenes میتوانند از طریق جریان خون، افراد سالم را دچار آرتریت septic کنند، اما تحقیقات نشان داده است کهدر اکثر افرادِ مبتال به آرتریت septic یک دلیل زمینهای وجود دارد. به مثالهای زیر توجه کنید:
بیماران مبتال به آرتریت روماتوئید به دالیل مختلفی از جمله التهاب مزمن مفاصل، مصرف کورتون، تخریب شدن ندولهای روماتوئیدی، زخمهای واسکولیتی و پوست پوشانندهی مفاصل دِفرمه، بیشترین درصد بروز )incidence( آرتریت عفونی
)غالباً ثانویه به )S.aureus را در مقایسه با سایر افراد دارند.
احتمال عفونت با S.aureus و باسیلهای گرم منفی و ایجاد شدن آرتریت septic در نتیجهی این عفونت در دیابتیها، دیالیزیها، افرادی که کورتون مصرف میکنند و یا سرطان دارند بیشتر است.
عامل ایجادکنندهی آرتریت septic در افرادی که از داروهای TNF inhibitor )مانند etanercept و )infliximab استفاده میکنند عفونت mycobacterial و یا سایر باکتریهای pyogenic میباشد.
عامل ایجادکنندهی آرتریت septic در افراد الکلی، افرادی که ضعف سیستم ایمنی هومورال دارند و افراد مبتال به هموگلوبینوپاتی عفونت پنوموکوکی میباشد.
شایعترین عوامل ایجادکنندهی آرتریت septic در افرادی که مبتال به HIV هستند عفونتهای پنوموکوکی، سالمونال و هموفیلوس آنفوالنزا میباشد.
احتمال عفونت mycobacterial و ایجاد شدن آرتریت septic در افرادی که نقص اولیهی ایمونوگلوبولین ) primary )immunoglobulin deficiency دارند زیاد است. اگر که آرتریت septic ایجاد شدهسریعاً درمان نشود )با دادن تتراسایکلین و تزریق وریدی ایمونوگلوبولین( میتواند آسیب دائمی در مفصل ایجاد شود.
احتمال عفونت با استافیلوکوک و استرپتوکوکهای فلور نرمال خودی در معتادانی که تزریق داخل وریدی دارند ) IV )drug users زیاد است. در آنها احتمال عفونت با سودوموناس و دیگر باکتریهای گرم منفی هم وجود دارد.
تظاهرات کلینیکی آرتریت عفونی یا septic :
در %۹۱ موارد، درگیری به صورت تک مفصلی است. مفصل زانو )knee( بیشتر از سایر مفاصل درگیر میشود، و بعد از آن به ترتیب مفصل ران )hip(، شانه )shoulder(، مچ )wrist( و آرنج )elbow( درگیر هستند. درگیری مفاصل کوچک دست
و پا معموالً به دنبال تلقیح مستقیم )direct inoculation( و یا گازگرفتگی حیوان ایجاد میگردد.
در IV drug user ها احتمال درگیری مفاصل محوری )axial( مانند ستون فقرات، sacroiliac و sternoclavicular
بیشتر از مفاصل محیطی )appendicular( است.
عفونت با درگیری چند مفصلی )polyarticular infection( بیشتر در افراد مبتال به آرتریت روماتوئید دیده میشود. فردی که گرفتار آرتریت septic است دارای عالئم زیر میباشد:
۱٫ درد متوسط تا شدید و دربرگیرندهی کل مفصل
۲٫ تجمع مایع )effusion(
۳٫ اسپاسم عضالت اطراف مفصل
۴٫ کاهش range of motion در تمام جهات
۵٫ تب ۳۸۸۳-۳۸۸۹( درجه و گاهی باالتر()در افرادی که آرتریت روماتوئید، نارسایی کبدی یا نارسایی کلیوی دارند و یا تحت درمان immunosuppressive هستند احتمال دارد که تب دیده نشود.(
معاینه بیماران مبتال به آرتریت عفونی یا septic :
مفاصل درگیر گرم، متورم و قرمز خواهند بود به جز مفاصل عمقیتر مانند hip، shoulder و deeply ( sacroiliac )situated joints که اینطور نیستند. در ضمن کاهش range of motion در تمام جهات دیده میشود.
تشخیص افتراقی: cellulitis، bursitis و acute osteomyelitis هر سه میتوانند تظاهرات بالینی شبیه به آرتریت septic داشته باشند. برای افتراق آنها از آرتریت septic باید بدانیم که؛ )۱ کاهش range of motion در آنها نسبت به آرتریت septic کمتر است و در تمامی جهات نیست )یعنی محدودیت حرکت کمتری دارند(، )۲ همچنین درگیری مفاصل به صورت لکالیزه میباشد برخالف آرتریت septic که به صورت درگیری کل مفصل بود.
عکسبرداری و بررسیهای آزمایشگاهی مربوط به آرتریت عفونی یا septic :
در تصویر رادیوگرافی گرفته شده از مفصلی که در مراحل اولیهی آرتریت septic است، تورم نسج نرم، فضای مفصلی افزایش یافته )به دلیل وجود مایع یا کشیدگی کپسول( و جابهجایی بافت نرم اطراف مفصل )به دلیل کشیدگی کپسول( دیده میشود.
بعد از گذشت دو هفته از شروع درگیری و تثبیت شدن عفونت در مفصل، کاهش فضای مفصلی و خوردگی مفصل )erosion( دیده میشود که نشاندهندهی عفونت پیشرفته و پروگنوز بد بیماری است.
از سونوگرافی برای دیدن تجمع مایع )effusion( در مفصل ران )hip( استفاده میشود. برای دیدن عفونت در ستون فقرات
و مفاصل sacroiliac و sternoclavicular، CT scan و MRI میتواند بسیار کمککننده باشد. در CBC افراد مبتال لکوسیتوز با شیفت به چپ و سطح افزایش یافتهی ESR و CRP دیده میشود.
در تمام بیماران مبتال به آرتریت septic قبل از شروع درمان آنتیبیوتیکی بایدحتماً آسپیراسیون مایع مفصلی و کشت خون ( چون شایعترین راه درگیری مفصل بود ) و کشت مایع مفصلی انجام داد. کشت خون ( B/C ) در حدود %۵۵ از افراد
مبتالیی که عامل ایجادکنندهی آرتریتشان S.aureus است مثبت میشود، در سایر افراد مبتال )منظور کسانی که عامل ایجادکنندهی آرتریتشان S.aureus نیست( این درصد کمتر است.
مایع مفصلی که آسپیره میشود کدر )turbid(، سرمی-خونی )serosanguineous( و گاهی چرکی )purulent( میباشد. اگر از این مایع مفصلی الم با رنگ آمیزی گرم تهیه کنیم، گلبولهای سفید )به خصوص PMN ها( را خیلی راحت میتوانیم ببینیم.
در آرتریت septic، سطح total protein و )lactate dehydrogenase( LDH مایع مفصلی افزایش و سطح گلوکز آن کاهش مییابد، البته این خیلی اختصاصی نیست و به منظور تشخیص آرتریت septic لزومی به انجام آن نمیباشد، به همین علت امروزه این روش دیگر کاربردی ندارد.
از آنجایی که تظاهرات بیماریهای مفصلیِ کریستالی )crystal-induced arthropathy( مانند نقرس )gout( و شبه نقرس )pseudogout( شبیه به آرتریت septic است و در آنها همانند آرتریت septic افزایش گلبولهای سفید دیده میشود، برای افتراقشان از هم باید مایع مفصلی را از لحاظ وجود کریستال چک کنیم.
در الم تهیه شده از مایع مفصلی، ارگانیسم عامل در %۷۵ موارد عفونت با S.aureus و %۳۱-۵۱ موارد عفونت با سایر باکتریها دیده میشود. یعنی اگر فرد آرتریت septic ناشی از S.aureus داشته باشد به احتمال %۷۵ این ارگانیسم در الم تهیه شده دیده خواهد شد.
کشت مایع مفصل در بیش از %۹۱مواردِ آرتریت septic مثبت خواهد بود.
در افرادی که دارای عفونت با باکتریهای سخت رشد )fastidious( هستند و یا آنتیبیوتیک مصرف کردهاند بهتر است برای کشت خونشان از محیط کشت liquid media استفاده کرد )به منظور داشتن کشتی بهتر(.
برای تشخیص عامل آرتریت septic در افرادی که به طور ناقص درمان شدهاند و یا جواب کشتشان منفی شده است میتوان از PCR کمک گرفت.
درمان آرتریت عفونی یا septic :
حتماً حتماً باید آسپیراسیون مایع مفصلی انجام شود و برای کشت و تهیه الم )smear( ارسال گردد تا در نهایت آنتیبیوتیک وسیعالطیف مناسب تجویز شود.
این بیماران نیاز به آسپیراسیون روزانهی مفصل دارند چراکه چرکی که تشکیل میشودسریعاً باعث تخریب مفصل میگردد )منم نفهمیدم .)
حاال یکمی هم راجع به آرتریت عفونی ناشی از N.gonorrhoeae صحبت کنیم…
اپیدمیولوژی آرتریت عفونی ناشی از N.gonorrhoeae )آرتریت گنوکوکی(:
اگر چه در کل بروز )incidence( آرتریت عفونی ناشی از گونوره کاهش یافته است اما این عامل همچنان علت %۷۱ از موارد آرتریت عفونی در افراد زیر ۴۱ سال است )شایعترین عامل(.
آرتریت ایجاد شده توسط N.gonorrhoeaeبه دنبال یک باکتریِمی ناشی از عفونت گنوکوکی و یا کلونیزاسیون مخاطی گنوکوکی بدون عالمت )asymptomatic gonococcal mucosal colonization( در urethra، cervix و pharynx ایجاد میگردد.
احتمال ()disseminated neisserial infection( DGIعفونت گنوکوکی منتشر( و آرتریت عفونی ناشی از N.gonorrhoeae در خانمها )به دلیل خونریزی )mense( و حاملگی( ۲ تا ۳ برابر آقایان است.
افرادی که نقص کمپلمان دارند، مستعد recurrent episodes of gonococcemia )اپیزودهای تکرارشوندهی گنوکوکی( هستند یعنی آن که احتمال بازگشت بیماری در آنها به صورت اپیزودیک زیاد است.
تظاهرات کلینیکی disseminated gonococcal infection (DGI) یا همان عفونت گنوکوکی منتشر:
شایعترین تظاهرات آن تب، لرز، راش و symptom های مفصلی میباشد.
بر روی تنهی افراد و سطح extensor اندامهای انتهایی آنها ممکن است تعداد کمی پاپول دیده شود که این پاپولها در نهایت به پوسچول خونریزیدهنده تبدیل خواهند شد.
ممکن است به صورت migratory arthritis )آرتریت مهاجر( و tenosynovitis در مفاصل زانو، دست، مچ، پا و مچ پا تظاهر کند.
سؤال: دلیل این تظاهرات پوستی و مفصلی چیست؟ به نظر میآید که دلیل آنها واکنش سیستم ایمنی به گنوکوکهای در حال گردش و کمپلکسهای ایمنی رسوب کرده باشد.
کشت مایع مفصلی در آنها همیشه منفی است، چرا؟ چون گفتیم که تظاهرات مفصلی آنها به دلیل واکنش سیستم ایمنی است و نه خود باکتری.
کشت خون در کمتر از %۴۵ افراد مبتال مثبت میشود.
در DGI به دلیل وجود التهاب انجام آسپیراسیون کمی سخت است. تعداد سلولهای مایع مفصلی به ۱۱۱۱۱-۲۱۱۱۱ سلول به ازای هر میکرولیتر میرسد.
نکته: آرتریت عفونی ناشی از N.gonorrhoeae یا همان آرتریت گنوکوکی با DGI )عفونت گنوکوکی منتشر( تفاوت دارد، طبق اینترنت آرتریت گنوکوکی به دنبال DGI میتواند ایجاد شود.
:gonococcal septic arthritis
نسبت به DGI شیوع کمتری دارد و تنها یک مفصل )ران، زانو، مچ پا و مچ دست( را درگیر میکند.
در آرتریت septic گنوکوکی انجام آسپیراسیون کار سختی نیست. تعداد سلولهای مایع مفصلی به بیشتر از ۵۱۱۱۱ سلول به ازای هر میکرولیتر میرسد.
این ارگانیسم در المهای تهیه شده به ندرت دیده خواهد شد. کشت مایع مفصلی در کمتر از %۴۱ افراد مبتال مثبت است.
کشت خونتقریباً همیشه منفی میباشد. کشت و الم تهیه شده از lesion های پوستیگاهاً میتواند مثبت شود.
محیط کشت مخصوص گنوکوک، thayer-martin agar نام دارد.
روش PCR برای تشخیص DNA های گنوکوکی موجود در مایع مفصلی حساسیت بسیار باالیی دارد.
در مواقعی که جواب کشت منفی شده است، کاهش چشمگیر عالئم فرد در عرض ۱۲ تا ۴۸ ساعت مصرف آنتیبیوتیک میتواند به تشخیص ما کمک کند.
آرتریت :)tuberculosis arthritis( TB
درگیری مفصلی در آن به صورت chronic granulomatous monoarthritis )تک مفصلی و مزمن( است. تنها %۱ از کل بیماران مبتال به سل )TB( گرفتار آرتریت TB میشوند.
:Poncet’s disease نوعی reactive arthritis است که به صورت polyarticular )چند مفصلی( و symmetric )قرینه( تظاهر مییابد. این بیماریمعموالً افرادی را که گرفتار توبرکلوز منتشر یا احشایی هستند درگیر میکند. در مفاصل مبتالیان به Poncet’s disease هیچ mycobacterium ای دیده نمیشود و این افراد با گرفتن درمان anti-TBسریعاً خوب میشوند. در این بیماری، مفاصل اندام تحتانی بیشتر درگیر است.
آرتریت TB بیشتر مفاصل تحمل کنندهی وزن ()weight-bearing joints(مانند hip، knee و )ankle را درگیر میکند.
مفاصل کوچکی که تحمل کنندهی وزن نیستند )non-weight-bearing joints( کمتر درگیر میشوند.
تورم monoarticular پیشرونده و درد ممکن است در طول ماهها تا سالها بعد بروز کند. تنها در نیمی از بیماران مبتال به آرتریت TB نشانههای سیستمیک دیده میشود.
همزمانی آرتریت TB و pulmonary TB باهم غیر معمول است.
در مایع مفصلی آسپیره شده ۲۱۱۱۱ سلول به ازای هر میکرولیتر دیده میشود که از این بین %۵۱ نوتروفیل هستند.
تهیه الم با رنگ آمیزی acid-fast انجام میشود و تنها در ۱/۳ موارد مثبت میشود. کشت مایع مفصلی در %۸۱-۹۱ موارد مثبت میشود. در مایع مفصلی التهاب گرانولوماتوز دیده خواهد شد.
روش PCR برای تشخیص TB بسیار به درد بخور است، چرا که کشت این باکتری مدت زمان زیادی میخواهد اما ما خیلی راحت با کمک PCR در عرض ۱-۲ روز بیماری را تشخیص میدهیم.
در تصویر رادیوگرافی، خوردگی مفاصل محیطی )peripheral joint erosion(، کاهش دانسیتهی استخوان اطراف مفصل )periarticular osteopenia( و کاهش فضای مفصلی دیده میشود.
درمان آرتریت TBدقیقاً همانند درمان pulmonary TB خواهد بود.
acute rheumatic fever :
تب روماتیسمی حاد بیماریایست که با سطح بهداشت و سطح اقتصادی-اجتماعی جامعه در ارتباط است. این بیماری، یک بیماری multi-organ است که در نتیجه ی واکنش ایمنی نسبت به استرپتوکوک گروه A به وجود می آید. با این که این بیماری می تواند اکثر قسمت های بدن را درگیر کند، ولی به جز درگیری دریچه های قلبی، همه ی موارد کامال برطرف می شوند. به عوارض ناشی از درگیری دریچه های قلبی rheumatic heart disease می گویند. این بیماری ارتباط مستقیمی با فقر دارد و تا قرن بیستم شیوع باالیی داشت که در سال های بعد، بخصوص در کشور های صنعتی، کاهش یافت که دلیل اصلی آن تراکم کمتر جمعیت، آنتی بیوتیک ها و افزایش سطح بهداشت بود. درسال ۰۸۹۱ اپیدمی از ARF در کوه های راکی در آمریکا روی داد. با این که ARF در کشور های توسعه یافته کاهش زیادی پیدا کرده، ولی همچنان در کشور های در حال توسعه شیوع باالیی دارد و شایع ترین عامل بیماری های قلبی در کودکان و یک فاکتور مهم در مرگ و میر بزرگساالن می باشد. تخمین زده می شود که حدود ۰۱ تا ۰۸ میلیون نفر در دنیا مبتال به ARF می باشند و حدود یک چهارم از یک میلیون مرگ در سال مربوط به ARF می باشد. امروزه %۸۱ از مرگ های ناشی از ARF در کشور های جهان سوم اتفاق می افتد. با وجود شیوع باالی بیماری در دنیا، در بعضی از نواحی این بیماری به صورت اندمیک وجود دارد که به آن hot spots می گویند )صحرای آفریقا، اقیانوس آرام، استرالیا و شبه قاره ی هند(.
این بیماری به طور معمول در سنین ۱ تا ۰۱ سال دیده می شود و معموال درگیری افراد باالی ۰۱ سال نادر است برخالف این حالت، اپیزود های تکرار شونده ی ARF در بالغین جوان و بزرگساالن است. Prevalence این بیماری بین ۵۱ تا ۱۱ سالگی است. از نظر جنس در ابتال به ARF هیچ تفاوتی بین زن ومرد وجود ندارد ولی در RHD این میزان در زنان دو برابر مرد ها می باشد.
پاتوژنز: سه عامل در پاتوژنز بیماری مطرح است:
۰٫ فاکتور های ارگانیسم: طبق شواهد ARF در اثر ابتال به فارنژیت و درگیری راه های هوایی فوقانی با استرپتوکوک گروه A ایجاد می شود. بعضی معتقدند که تمام سوش ها استرپتوکوک گروه A می تواند ایجاد بیماری کنند همچنین ارتباطی بین عفونت های پوستی و استرپتوکوک های گروه C و G در ایجاد ARF پیدا شده.
۵٫ فاکتور های میزبان: ۰ تا ۶ درصد جمعیت مستعد ابتال به ARF هستند. افزایش ابتال به ARF و بخصوص کره، بیانگر این مسئله است که احتماال ویژگی ژنتیکی )آلل های کالس دو )HLA میزبان یک فاکتور تعیین کننده برای ابتال به این بیماری می باشد. همچنین در افرادی که سابقه ی ابتال به ARF را دارند، سطح باالیی از آلوآنتیژن در سطح سلول های لنفوست B دیده می شود.
صفحه ۱۱ از ۱۱
۰٫ پاسخ ایمنی: اپیتوپ های A، B و C در پروتئین M وجود دارند. این پروتئین روی غشا و یا دیواره ی سلولی باکتری قرار دارد که شبیه مولکول هایی از قبیل میوزین، تروپومیوزین، اکتین، کراتین، المینین، ویمنتین و -Nاستیل گلوکزآمین می باشد. این مسئله باعث به وجود آمدن cross reaction می شود. در درگیری دریچه های قلبی، عالوه بر میوزین، المینین هم درگیر می شود. برخی شواهد نشان می دهند که آنتی بادی های تولید شده برعلیه باکتری ها باعث آسیب دریچه ای در افراد مبتال می شوند.
حال اگر شخصی که از نظر ژنتیکی مستعد ابتال به ARF است در محیط هایی مثل سربازخانه، مهدکودک، خانواده ی پرجمعیت و … قرار بگیرد دچار ARF می شوند.
عالئم کلینیکی: دوره ی کمون ARF بین ۰ و ۱ هفته )به طور متوسط سه هفته می باشد.( البته کره و کاردیت دوره ی کمون باالتری دارند و ممکن است تا ۶ ماه برسد. بسیاری از بیماران سابقه ای از گلو درد را گزارش می کنند. به این دلیل که بیمار ممکن است سابقه ی گلودرد را فراموش کرده باشد، تنها راه قطعی تشخیص، پیدا کردن آنتی بادی در خون می باشد. از نظر کلینیکی شایع ترین تظاهر این بیماری پلی آرتریت ۶۱( تا )% ۵۱ و تب ۱۱( تا )% ۶۱ می باشد. کره در ۵ تا % ۰۱ وerythema marginatum و ندول های زیر جلدی کمتر از %۱ دیده می شوند.
درگیری قلبی: بیشتر از %۶۱ افرادی که دچار ARF شده اند، مبتال به RHD می شوند. آسیب دریچه مشخصه ی RHD است. دریچه ی میترال اغلب درگیر است و ممکن است گاهی با درگیری دریچه ی آئورت همراهی داشته باشد، در موارد نادر ممکن است فقط دریچه ی آئورت درگیر باشد. در مراحل اولیه ی بیماری معموال فقط دریچه نارسا می شود و بعد به مرور زمان دچار کلسیفیکاسیون و تنگی می شود. درگیری پریکارد درRHD به صورت درد قفسه ی سینه نمایان می شود که با اکوکاردیوگرافی قابل تشخیص است. ممکن است که در این افراد میوکاردیت دیده شود که معموال با اختالالت هدایتی است
و در این افراد PR interval زیاد می شود همچنین انواعی از بلوک های قلبی قابل مشاهده است و صدای اول قلب در این افراد زیاد می شود.
درگیری مفصل: درگیری مفصلی در ARF به دو شکل دیده می شود، یکی از آن ها که ماژور محسوب می شود پلی آرتریت است که معموال مفاصل گرم، قرمز، متورم و حساس است و این مسئله محدوده ی حرکت مفصل را کاهش می دهد. درگیری معموال به صورت چند مفصلی و مهاجر است و همچنین مفاصل بزرگ مثل زانو، آرنج، مچ و … در ARF درگیر می شوند که معموال غیر قرینه است. درد در این شرایط بسیار شدید و ناتوان کننده است که با تجویز ضدالتهاب ها کاهش می یابد. از عالئم مینور می توان به آرترالژی اشاره کرد که در آن مفاصل التهاب ندارند در این حالت نیز مفاصل بزرگ به صورت مهاجر درگیر می شوند. چون ممکن است اولین عالمت ARF آرترالژی باشد، شناسایی آن و تجویز به موقع ضدالتهاب ها می تواند روند بیماری را تغییر دهد.
یکی از خصوصیات درگیری مفاصل در ARF این است که بسیار خوب به سالیسیالت ها و NSAIDs ها جواب می دهند. بعد از گذشت یک تا دو روز از تجویز این دارو ها عالئم بیماری از بین می رود و به غیر از درمان در تشخیص هم کمک کننده است. چون این دارو ها عالئم بیماری را از تا حدودی مخفی می کنند، توصیه می شود که در کودکانی که تب و آرتریت دارند به جای این دارو ها از استامینوفن و یا کدئین استفاده شود تا زمانی که تشخیص قطعی برای ARF داده شود.
syndromes chorea : به دلیل دوره ی کمون طوالنی کره، معموال زمانی ظاهر می شود که دیگر عالئم ARF دیده نمی شوند. کره در زنان بیشتر دیده می شود و می تواند فقط سر )مثال حرکت کردن زبان( و اندام فوقانی را درگیر کند یا به صورت generalized در تمام بدن دیده شود. اگر عالئم کره، فقط در قسمت خاصی از بدن دیده شود به آن hemichorea می گویند. کره می تواند با شدت های متفاوتی دیده شود، در کودکان معموال با شکایت از تغییر دست خط به پزشک مراجعه می کنند. در موارد خفیف، شخص توانایی انجام کار های ظریف مثل بستن دکمه را ندارد. گاهی ممکن است که حرکات پرتابی حاصل از کره به قدری شدید باشد که زندگی شخص را مختل کند ولی تا ۶ هفته همه ی نشانه های کره از بین می رود.
:erythema marginatum در ARF دیده می شود، به صورت ضایعات صورتی رنگ با مرکز رنگ پریده دیده می شود که معموال از محیط منتشر می شوند. بیشتر روی تنه و کمتر روی اندام ها دیده می شود و هیچ موقع صورت را درگیر نمی کند.
ندول های زیر جلدی: توده های زیر جلدی کوچک، بدون درد با اندازه ی ۱٫۱ تا ۵ سانتی متر می باشند که روی برجستگی های استخوانی )دست، پا، occiput، آرنج و گاهی ستون مهره( را می پوشاند. این تظارات تاخیری می باشند چون دو تا سه هفته بعد از بیماری به وجود می آیند و به مدت سه هفته ادامه پیدا می کنند. اهمیت این ندول ها، در همراهی آن ها با کاردیت است.
سایر تظاهرات :ARF تب یکی از عالئم می باشد که اکثرا دیده می شود، به ندرت تب و کره با هم دیده می شوند. با این که اکثرا دمای بدن بیمار ۰۸ درجه است ولی تب های کمتر از این هم ناشایع نیست. CRP و ESR در این افراد افزایش پیدا میکند و همچنین لوکوسیتوز در این افراد دیده می شود.
برای تشخیص ARF باید به تظاهرات توجه کنیم، کره و کاردیت چون دوره ی کمون باالیی دارند در تشخیص این بیماری کمک کننده نیستند همچنین در بسیاری از مواقع کشت باکتری منفی می شود به همین دلیل از تست های سرولوژی برای تشخیص استفاده می شود. شایع ترین تست سرولوژی )ASO( Antistreptolysin O و )ADB( Anti-DNase B می باشد.
به دنبال عفونت استرپتوکوکی دو سندرم دیده می شود. یکی از آن ها poststreptococcal reactive arthritis )PSRA( است، این آرتریت متفاوت از ARF می باشد. در این سندرم برخالف ARF مفاصل کوچک و به صورت قرینه درگیر می شوند، دوره ی کمون کوتاه )کمتر از یک هفته( دارند. به ندرت ممکن است که با استرپتوکوک های غیر از گروه A ایجاد شوند. پاسخی که PSRA به سالیسیالت ها می دهند پاسخ آهسته ای است و در این بیماران معموال کاردیت دیده نمی شود.
Pediatric autoimmune neuropsychiatric disorders associated with Streptococcal infections (PANDAS) یک اختالل autoimmune که در اثر عفونت استرپتوکوکی در بچه ها دیده می شود که
شامل طیفی از عالئم مثل تیک و اختالالت وسواسی می باشد که معموال با کاردیت همراهی ندارد.
جدول زیر مهم است.

به اضافه ی معیار های تشخیصی که در شکل باال آمده است، اگر بیمار حمالت تکراری از عفونت را با بیماری دریچه ای قلبی اثبات شده داشته باشد، دو تا معیار مینور با شواهد عفونت استرپتوکوکی برای تشخیص کافی است. در حالتی که شخص کره و اختالل دریچه ای داشته باشد، نیازی به معیار دیگری برای تشخیص نیست.
استفاده از اکو هم به صورت basic و هم به صورت دوره ای در تشخیص و تعیین میزان بیماری کمک کننده است. اگر بیمار تب دارد باید حتما کشت خون انجام شود تا بتوان اندوکاردیت را رد کرد. از ECG برای مشخص کردن اختالالت ریتمی به مدت دو هفته و دو ماه بعد از مواجهه استفاده می شود. اگر شواهد کلینیکی به نفع کاردیت باشد، باید برای مریض درخواست X-RAY بدهیم. قبل از تجویز آنتی بیوتیک حتما باید بزای بیماران کشت حلق صورت بگیرد. برای بیماران باید تیتر ASO و ADB اندازه گیری شود و در صورت نرمال بودن این تست ها، باید ۰۱ تا ۰۱ روز بعد دوباره این تست ها انجام شود.
تشخیص هایی افتراقی: چون در اندوکاردیت شخص با تب و آرتریت مراجعه می کند به همین دلیل برای افتراغ باید از کشت خون استفاده کنیم. اگر درگیری مفصل به صورت تکی باشد، به دلیل تشابه با آرتریت سپتیک حتما باید مایع مفصل آسپیره شود. کره در بیماری ویلسون هم دیده می شود و برای تمایز باید ceruloplasmin خون را اندازه گرفت همچنین در لوپوس هم می توان حرکاتی مانند کره دید به همین دلیل باید میزان ANA را اندازه گیری کرد. مصرف بعضی از دارو ها می توانند عالئم کره را ایجاد کند به همین دلیل شرح حال دارویی مهم است.
برای ARF اگر قلب درگیر باشد باید درمان شود، در بقیه ی موارد درمان فقط به صورت عالمتی است.
برای پیشگیری از ایجاد ARF طبق جدول زیر عمل می کنند:


